Investigadores del Consejo Superior de Investigaciones Científicas (CSIC) han demostrado que la proteína CTCF "es esencial para la correcta regulación de los genes responsables del desarrollo embrionario", analizando por primera vez la función de esta proteínas in vivo durante el desarrollo embrionario de un animal en su etapa de formación de órganos y del patrón corporal. De esta forma, el artículo publicado en Nature Communications, "abre nuevas vías de estudio", explican desde el CSIC.
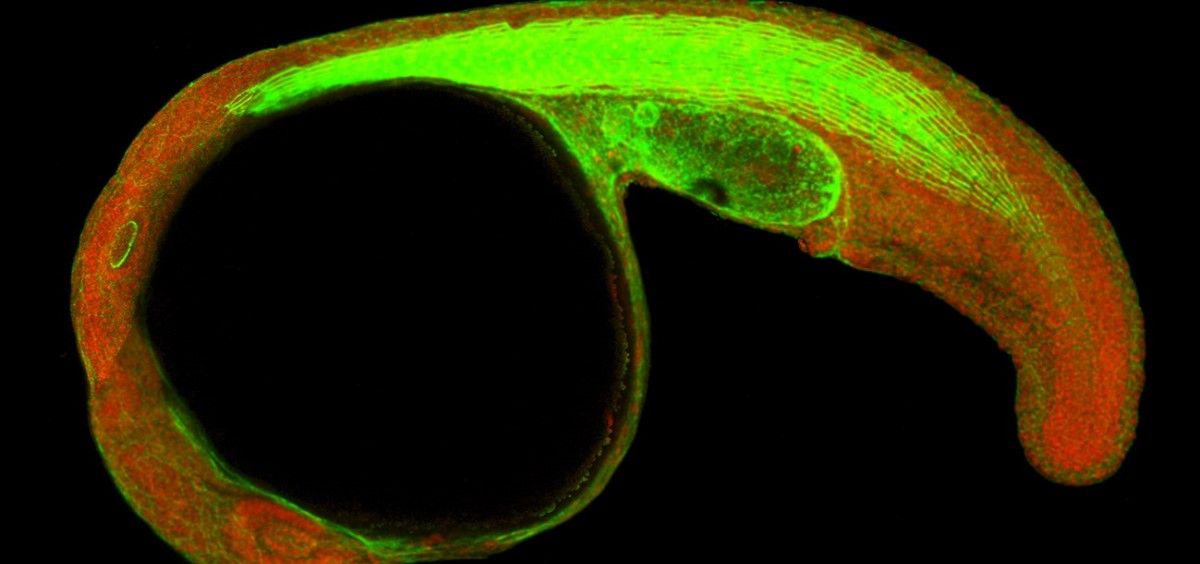
Esta investigación ha utilizado al pez cebra como modelo para conocer el papel que juega la estructura tridimensional del genoma en la regulación de la expresión de los genes durante el desarrollo embrionario. En palabras del investigador del Centro Andaluz de Biología del Desarrollo (CABD), José María Santos Pereira, "aproximadamente el 98% del genoma humano es ADN no codificante, es decir, no contiene genes. Pero, al contrario de lo que se pensó originalmente, gran parte de este ADN no codificante tiene una función".
En este sentido, añade que "una parte del ADN no codificante está ocupado por lo que llamamos elementos reguladores, que son secuencias de ADN que, tomando prestada la metáfora que solía usar José Luis (rse refiere a José Luis Gómez Skarmeta, investigador del centro y fallecido hace un año), funcionan como interruptores que 'apagan' o 'encienden' a los genes. Esto ocurre así en todos los vertebrados, como el pez cebra, que comparte aproximadamente un 70% de genes con el ser humano”.
"Gracias a este modelo, hemos averiguado que CTCF es esencial para la correcta regulación de los genes responsables del desarrollo embrionario"
De esta forma, durante el desarrollo embrionario - proceso que lleva a una célula a convertirse en un animal -, "es cuando la regulación de la expresión de los genes alcanza su mayor complejidad y esto ocurre así gracias a que los genes responsables del desarrollo están controlados por múltiples de estos interruptores", informan desde el CSIC.
“Aunque en muchos casos los interruptores se encuentran a largas distancias de sus genes diana en la secuencia lineal de la hebra de ADN, en los últimos años se ha demostrado que el genoma se pliega tridimensionalmente como una madeja de lana, facilitando el contacto de los interruptores con los genes a los que regulan”, comenta Santos. En los mamíferos, se ha demostrado que esta proteína CTCF es clave para el plegamiento 3D del genoma, aunque su función durane el desarrolo embrionario no se había podido estudiar hasta el momento. Gracias a la utilización del pez cebra como modelo, los investigadores han sido "capaces de superar esta limitación".
“Gracias a este modelo, hemos averiguado que CTCF es esencial para la correcta regulación de los genes responsables del desarrollo embrionario. ¿Cómo lo hace? Pues CTCF se une al ADN y actúa a modo de barrera delimitando las zonas dentro de las cuales pueden actuar los interruptores. En otras palabras, es como si dividiéramos la madeja de lana en una serie de ovillos consecutivos, separados unos de otros. Esto favorece que los interruptores 'enciendan' o 'apaguen' a sus genes diana y evita que enciendan o apaguen a otros que no les corresponde”, sostiene el científico.
El pez cebra es un modelo ideal para estudiar la pérdida de función de genes humanos que conduce a patologías congénitas
Así, los investigadores del centro observaron que "cuando CTCF no está, la ausencia de estas barreras elimina los pequeños ovillos y debilita el contacto de los interruptores con sus genes diana, al mismo tiempo que se forman nuevos contactos con otros genes, traspasando los límites que normalmente establece CTCF. Esto provoca que se desregulen genes muy importantes en el desarrollo, de hecho, cientos de ellos, y a su vez los genes que dependen de estos, dando lugar a miles de genes con expresión incorrecta", apunta el CSIC.
La generación de este mutante de CTCF en pez cebra mediante la tecnología CRISPR de edición génica ha aportado un nuevo modelo con el que profundizar en la función de CTCF in vivo, durante el desarrollo embrionario animal, en futuros estudios. “Por ejemplo, la utilización de tecnologías de célula única en nuestro modelo podría permitirnos averiguar cuál es el impacto de la pérdida de CTCF en los distintos tipos celulares y órganos presentes en el embrión, es decir, si su función es más importante en unos tipos celulares que en otros y por qué”, señala Santos Pereira. También refuerza la idea de que el pez cebra es un modelo ideal para estudiar la pérdida de función de genes humanos que conduce a patologías congénitas.
La investigación ha sido financiada por ERC Advanced Grant, el Ministerio de Ciencia e Innovación, la Unidad de Excelencia María de Maeztu GEM-DMC2 y la Junta de Andalucía, entre otros.