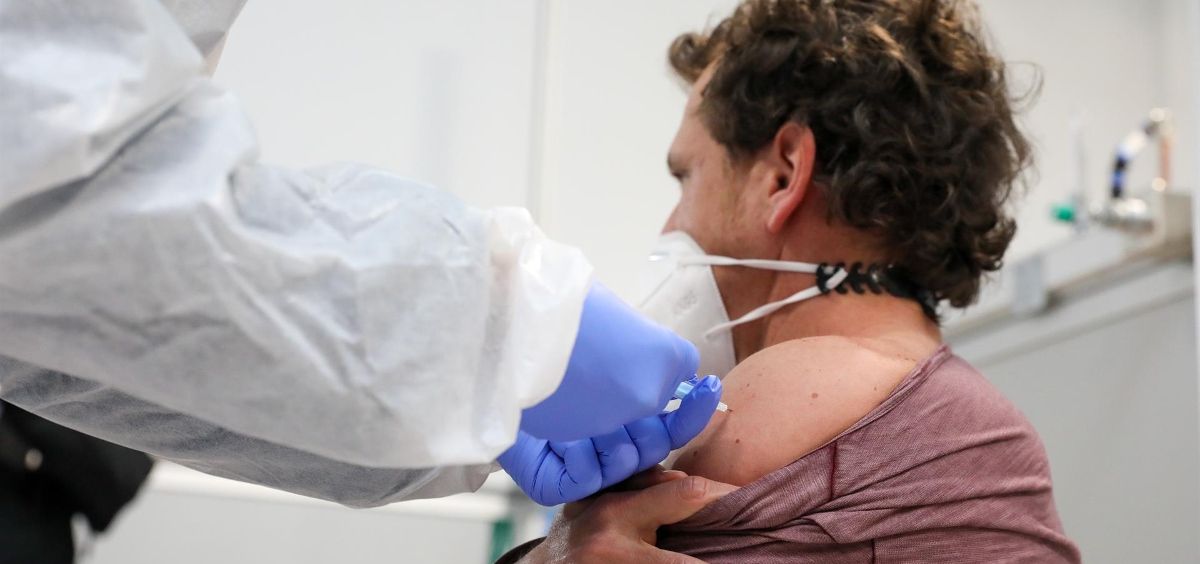
Efecto dominó. Esta es la mejor forma para definir la situación que se ha vivido en Europa con la vacuna contra la Covid-19 desarrollada por AstraZeneca y la Universidad de Oxford. El pasado lunes 15 de marzo la ministra de Sanidad, Carolina Darias, convocaba con carácter de urgencia a las comunidades autónomas a una reunión extraordinaria del Consejo Interterritorial del Sistema Nacional de Salud (CISNS) para suspender, de forma “inmediata y preventiva” la vacunación con la vacuna de AstraZeneca en España durante los próximos 15 días. Una decisión que se producía después de que Dinamarca, Austria, Países Bajos, Alemania, Francia y otros países europeos paralizasen la administración de esta vacuna tras detectarse varios casos de trombosis en personas que habían recibido el suero.
Un duro golpe para las campañas nacionales de inmunización frente a la Covid-19 en el viejo continente, y que pone contra las cuerdas al laboratorio anglosueco cuya imagen ya estaba dañada tras reconocer que solo podrá entregar a los países de la Unión Europea 100 millones de dosis durante el primer semestre del año.
Ahora todos los ojos están puestos en el Comité de Evaluación de Riesgos en Farmacovigilancia (PRAC, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés), responsable de analizar los eventos trombóticos acaecidos en los últimos días en personas que habían recibido la vacuna de AstraZeneca.
Emer Cooke, directora gerente de la EMA, aseguraba este martes en una rueda de prensa que el organismo está evaluando “en profundidad” los casos que se han producido de coágulos y que han sido detectados por los Estados miembros con el objetivo de determinar si su aparición guarda relación con la administración de la vacuna o se trata de “coincidencias”. En este sentido la EMA se ha mostrado “firmemente convencida” de que los beneficios que aporta la vacuna superan los riesgos de posibles efectos secundarios recalcando que, por el momento, no se han encontrado “indicios” que demuestren la vinculación de la aparición de trombosis con la inoculación del suero.
"Todavía estamos firmemente convencidos de que los beneficios de la vacuna de AstraZeneca para prevenir la Covid-19 con sus riesgos asociados de hospitalización supera los riesgos de los efectos secundarios", ha manifestado. "En la actualidad no hay indicios de que la vacunación haya causado estas condiciones".
"En la actualidad no hay indicios de que la vacunación haya causado estas condiciones"
No obstante, Cooke ha indicado que las “preocupaciones” que se han generado en los últimos días relativas a la seguridad de la vacuna merecen una “evaluación científica” para estudiar “en detalle todos los casos identificados”. Los resultados de los análisis de los casos se harán públicos el próximo jueves. Ha explicado que este tipo de situaciones se contemplan en las campañas de vacunación ya que estas no están exentas de lo que ha calificado como “incidentes”. En este sentido ha puesto en valor el papel de la EMA para evaluar si se trata de coincidencias o realmente existe un vínculo entre la administración de la vacuna los episodios de trombosis.
DATOS SIMILARES EN OTRAS VACUNAS
La EMA investigó en un primer momento la posibilidad de que los casos de trombosis estuviesen relacionados con la administración de un lote de la vacuna. Una opción que fue descarta tras reportarse episodios en personas vacunadas con dosis pertenecientes a distintos lotes.
Desde el organismo dejan claro que, aunque en estos momentos se están investigando los casos de las personas vacunadas con AstraZeneca, la EMA evalúa “posibles efectos adversos” en todas las vacunas que han recibido su autorización. En este sentido explican que “parece haber números similares” de problemas sanguíneos. "Ahora el foco lo tenemos en AstraZeneca por los incidentes detectados en Europa, pero hemos mirado las tasas de todas las vacunas actualmente en circulación y parece que hay números similares apareciendo en todo el mundo”, explica tal y como recogen en Europa Press.
ASTRAZENECA: ‘NO EXISTE NINGUNA EVIDENCIA’
La compañía emitía el 15 de marzo un comunicado a través del que recalcaba que la seguridad es de “primordial importancia”, por lo que “analizan constantemente la seguridad” de su vacuna.
Una minuciosa revisión de todos los datos de seguridad disponibles de más de 17 millones de personas vacunadas en la Unión Europea (UE) y el Reino Unido con la vacuna frente a la Covid-19 de AstraZeneca “ha mostrado que no existe ninguna evidencia de un aumento del riesgo de embolia pulmonar, trombosis venosa profunda (TVP) o trombocitopenia en ningún grupo de edad definido, sexo, lote o en ningún país concreto”.
"No existe ninguna evidencia de un aumento del riesgo de embolia pulmonar, trombosis venosa profunda (TVP) o trombocitopenia en ningún grupo de edad definido, sexo, lote o en ningún país concreto”
“Hasta ahora, en la UE y el Reino Unido, se han notificado 15 casos de TVP y 22 de embolia pulmonar entre las personas que recibieron la vacuna, según los casos recibidos por la compañía hasta el 8 de marzo. Esta cifra es muy inferior a la que se esperaría que ocurriera de forma natural en una población general de este tamaño y es similar a la de otras vacunas autorizadas frente a la Covid-19. El informe mensual de seguridad se hará público en la página web de la Agencia Europea del Medicamento durante la semana próxima, de conformidad con las medidas excepcionales de transparencia para la Covid-19”, informan.
“Alrededor de 17 millones de personas en la UE y el Reino Unido han recibido ya nuestra vacuna, y el número de casos de coágulos sanguíneos notificados en este grupo es inferior a los cientos de casos que cabría esperar entre la población general. La naturaleza de la pandemia ha hecho que se preste una mayor atención a los casos individuales y estamos yendo más allá de las prácticas habituales de monitorización de la seguridad de los medicamentos autorizados al notificar los acontecimientos relacionados con la vacuna, para garantizar la seguridad pública”, explica Ann Taylor, jefa médico de AstraZeneca.
ESPAÑA NO CAMBIA ‘POR AHORA’ EL CALENDARIO VACUNAL
En la rueda de prensa posterior al Consejo de Ministros de este martes la portavoz del Gobierno y ministra de Hacienda, María Jesús Montero, recordaba que la decisión de suspender la vacunación con AstraZeneca en España es “temporal y cautelar”.
“No se va a producir por ahora ningún tipo de alteración en el calendario vacunal previsto ni sustitución definitiva de esta vacuna. Todo esto sería prematuro”
“Se trata de una incidencia muy baja (en relación a los casos de trombosis en personas vacunadas) pero el hecho de que sean las vacunas en este preciso momento medicamentos que acaban de ponerse en producción y han tenido un periodo acortado de monitorización de los efectos en las diferentes fases de los ensayos, es lo que estrecha la labor de farmacovigilancia en nuestro país y en la Unión Europea. A partir de este mecanismo es farmacovigilancia es como conocemos estos episodios”, ha asegurado dejando claro que “todavía no hay evidencia de que hayan sido producidos por la vacuna”.
Montero trasladaba un mensaje de “absoluta tranquilidad” y aseverando que “no se va a producir por ahora ningún tipo de alteración en el calendario vacunal previsto ni sustitución definitiva de esta vacuna. Todo esto sería prematuro”.
LA VACUNA DE ASTRAZENECA
La vacuna frente a la Covid-19 de AstraZeneca fue desarrollada conjuntamente por la Universidad de Oxford y su compañía asociada, Vaccitech. La vacuna utiliza un vector viral de chimpancé no replicativo basado en una versión debilitada de un virus del resfriado común (adenovirus) que causa infecciones en los chimpancés y contiene el material genético de la proteína de la espícula del virus SARS-CoV-2. Después de la vacunación, se produce la proteína superficial de la espícula, lo que prepara al sistema inmunitario para atacar al virus SARS-CoV-2 si posteriormente infecta al organismo.
La vacuna ha recibido la autorización de comercialización condicional o uso de emergencia en más de 70 países de los seis continentes, y con la reciente inclusión en la lista de uso de emergencia presentada por la Organización Mundial de la Salud acelera el camino para su acceso en hasta 142 países a través de la plataforma COVAX.